11 Oct Ramucirumab la alternativa en segunda línea para pacientes con cáncer gástrico evidencia clínica y de mundo real
Tiempo de lectura: 6 minutosEl cáncer gástrico es la quinta neoplasia maligna más común y la tercera causa principal de mortalidad por cáncer en todo el mundo. Actualmente, las combinaciones basadas en platino y fluoropirimidina se aceptan como regímenes farmacológicos establecidos de primera línea. No hay muchas opciones de tratamiento después del fracaso de la terapia de primera línea. En ensayos aleatorizados, la quimioterapia de segunda línea seleccionada mejoró significativamente la supervivencia general en comparación con el mejor tratamiento estándar; sin embargo, la mediana de supervivencia fue inferior a 6 meses. Por lo tanto, se necesitan nuevas opciones de tratamiento de segunda línea más activas.1
La señalización y la angiogénesis mediadas por VEGF y VEGFR-2 contribuyen a la patogénesis del cáncer gástrico. En pacientes con cáncer gástrico, los niveles circulantes de VEGF se asocian con una mayor agresividad tumoral y una supervivencia reducida. En modelos animales de adenocarcinoma gástrico, la inhibición de VEGFR-2 redujo el crecimiento tumoral y la vascularización. Ramucirumab,es un anticuerpo monoclonal humano IgG1 antagonista de VEGFR-2, previene la unión del ligando y la activación de la vía mediada por el receptor en las células endoteliales.
Se eligió paclitaxel para la combinación en base a ensayos de segunda línea con un solo agente; los resultados de un análisis retrospectivo en el cáncer gástrico indicaron una eficacia similar entre los fármacos de segunda línea de uso frecuente (taxanos o irinotecán); en un ensayo aleatorizado japonés, el paclitaxel semanal se asoció con un buen perfil de toxicidad en comparación con irinotecán como terapia de segunda línea en pacientes con cáncer gástrico.1
Sobre la base de estos antecedentes, se diseñó un ensayo de fase 3, doble ciego, controlado con placebo denominado RAINBOW con la finalidad de evaluar la seguridad y la eficacia de la combinación de ramucirumab más paclitaxel en pacientes con adenocarcinoma gástrico avanzado o adenocarcinoma de la unión gastroesofágica con progresión de la enfermedad después de utilizar quimioterapia combinada como tratamiento de primera línea.1
Entre el 23 de diciembre de 2010 y el 23 de septiembre de 2012, 665 pacientes fueron asignados aleatoriamente al tratamiento: 330 a ramucirumab más paclitaxel y 335 a placebo más paclitaxel. La supervivencia global fue significativamente mayor en el grupo de ramucirumab más paclitaxel que en el grupo de placebo más paclitaxel (mediana de 9,6 meses [IC del 95 % 8,5–10,8] frente a 7,4 meses [IC del 95 % 6,3– 8·4], razón de riesgo 0·807 [IC 95% 0·678–0·962], p=0·017) (Figura 1). Los eventos adversos de grado 3 o superior que ocurrieron en más del 5 % de los pacientes en el grupo de ramucirumab más paclitaxel versus placebo más paclitaxel incluyeron neutropenia (133 [41 %] de 327 versus 62 [19 %] de 329), leucopenia (57 [17 %] frente a 22 [7%]), hipertensión (46 [14%] frente a ocho [2%]), fatiga (39 [12%] frente a 18 [5%]), anemia (30 [9%] frente a 34 [ 10 %]) y dolor abdominal (20 [6 %] frente a 11 [3 %]). La incidencia de neutropenia febril de grado 3 o superior fue baja en ambos grupos (diez [3 %] frente a ocho [2 %]).1
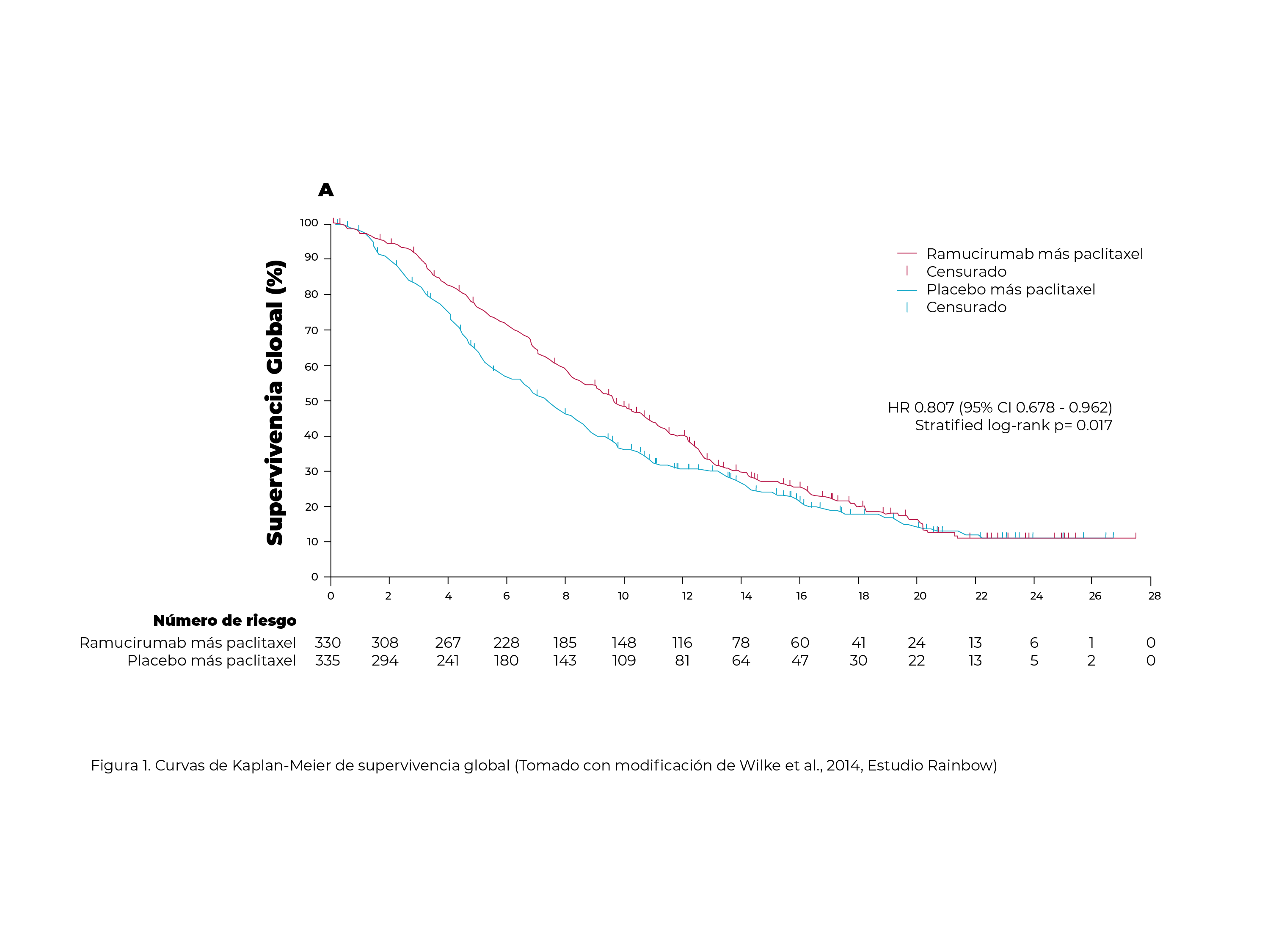
Sobre la base de estos resultados se concluyó que la combinación de ramucirumab con paclitaxel aumenta significativamente la supervivencia global en comparación con placebo más paclitaxel, y podría considerarse como un nuevo tratamiento estándar de segunda línea para pacientes con cáncer gástrico avanzado.1
Varios procesos de señalización oncogénica han sido implicados en el desarrollo del cáncer gástrico. Los hallazgos con los anticuerpos monoclonales trastuzumab y ramucirumab sugieren que las vías de señalización de HER2 y VEGF podrían ser objetivos válidos para la terapia del cáncer gástrico. RAINBOW muestra que, en pacientes con adenocarcinoma gástrico progresivo o adenocarcinoma gastroesofágico después de la terapia estándar de primera línea, ramucirumab en combinación con paclitaxel puede aumentar significativamente la supervivencia global en comparación con placebo más paclitaxel. Junto con un ensayo anterior de fase 3 de ramucirumab como agente único en cáncer gástrico avanzado de segunda línea, los resultados de estos estudios respaldan el papel de una terapia dirigida al receptor VEGF y tal vez la adición de un nuevo agente a los tratamientos y el estándar de atención en esta población de pacientes.1
Recientemente se condujo el estudio RAMOSS, cuyo objetivo evalúa el perfil de seguridad y eficacia de ramucirumab en el “entorno de la vida real”. Para lograr estos objetivos, pacientes de 25 hospitales italianos iniciaron una terapia consistente en ramucirumab 8 mg/kg i.v. d1,15q28 con o sin paclitaxel 80 mg/m2 i.v. d1,8,15q28. El criterio de evaluación principal fue la seguridad y los objetivos secundarios fueron la tasa de respuesta global (ORR), la supervivencia libre de progresión (PFS) y la supervivencia global (OS).2
Ciento sesenta y siete pacientes con progresión de la enfermedad en el tratamiento de primera línea recibieron ramucirumab como monoterapia (10 %) o combinado con paclitaxel (90 %). La mediana de duración del tratamiento fue de 4 meses (1-17 meses). La incidencia global de toxicidad de grado (G) 3-4 fue del 9,6 % y de neutropenia del 5,4 %; el tratamiento se interrumpió por toxicidad en el 3% de los pacientes. Los eventos adversos (EA) más frecuentes fueron fatiga G1-2 (27,5 %), neuropatía G1-2 (26,3 %) y neutropenia G1-2 (14,9 %). La ORR fue del 20,2 %. Se observó enfermedad estable en el 39,2 % de los pacientes, con una tasa de control de la enfermedad del 59,4 %. Con una mediana de seguimiento de 11 meses, la mediana de PFS fue de 4,3 meses (intervalo de confianza [IC] del 95 %: 4,1–4,7), mientras que la mediana de OS fue de 8,0 meses (IC del 95 %: 7,09–8,9) (Figura 2 & 3).
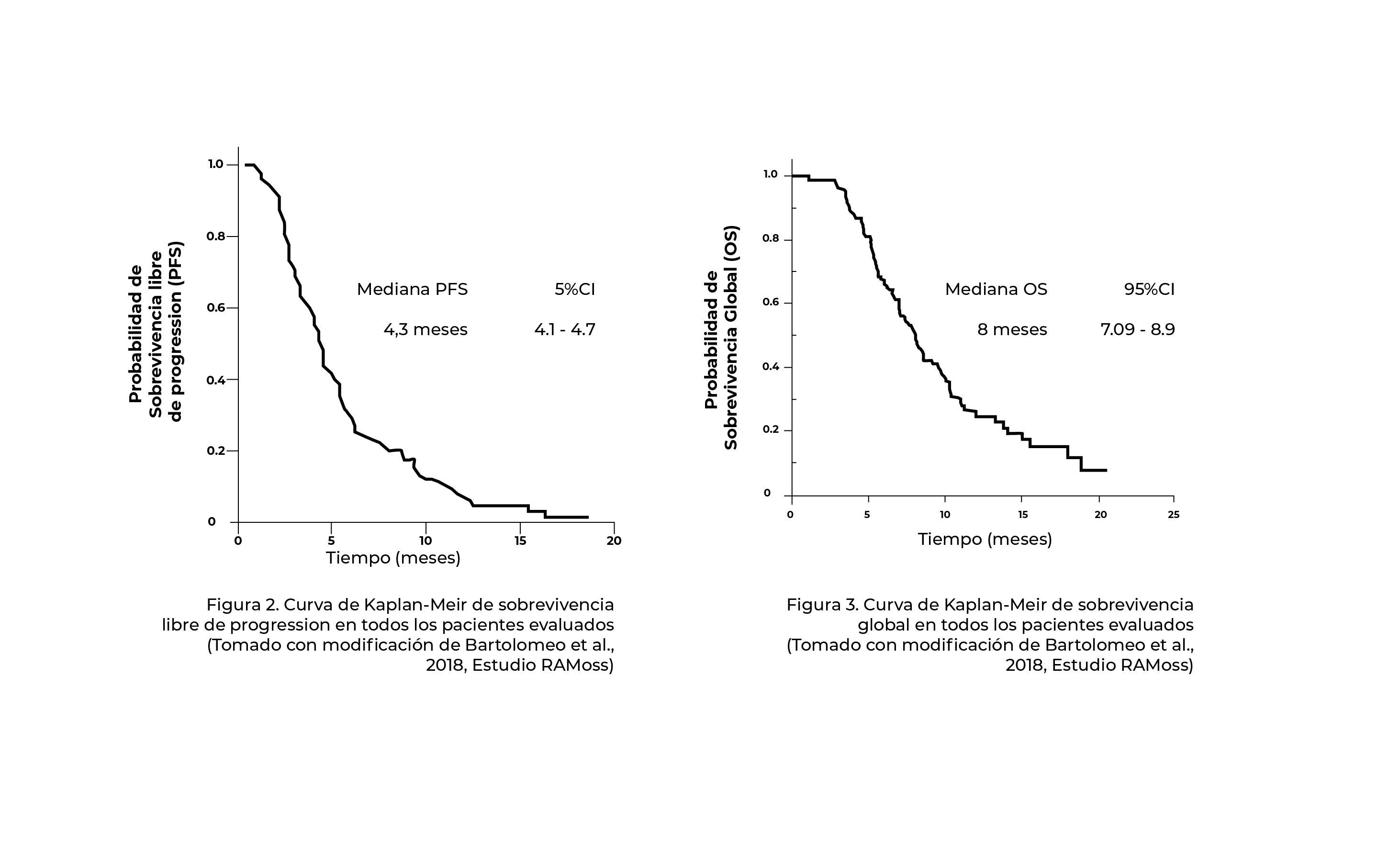
En un análisis multivariado, el estado funcional ECOG <1 o ≥1 (HR 1,13, IC 95 % 1,0–1,27, p = 0,04) y la presencia versus ausencia de metástasis peritoneales (HR 1,57, IC 95 % 1,63–2,39, p = 0,03) fueron factores independientes de mal pronóstico.2
En pacientes con tumores positivos para HER2, la mediana de PFS y OS fue de 4,4 y 7,9 meses, respectivamente. La Figura 3 muestra la OS y la PFS según el programa de tratamiento: la mediana de SG fue de 8,3 meses (IC 95 % 7,2–8,8) y la mediana de PFS fue de 4,5 meses (IC 95 % 4,1–4,8) para los pacientes tratados con ramucirumab y paclitaxel; la mediana de OS fue de 4,8 (IC del 95 %: 2,8–12,3) y la mediana de PFS fue de 2,7 meses (IC del 95 %: 0,9–6,1) para los pacientes tratados con monoterapia con ramucirumab (Figura 4).2
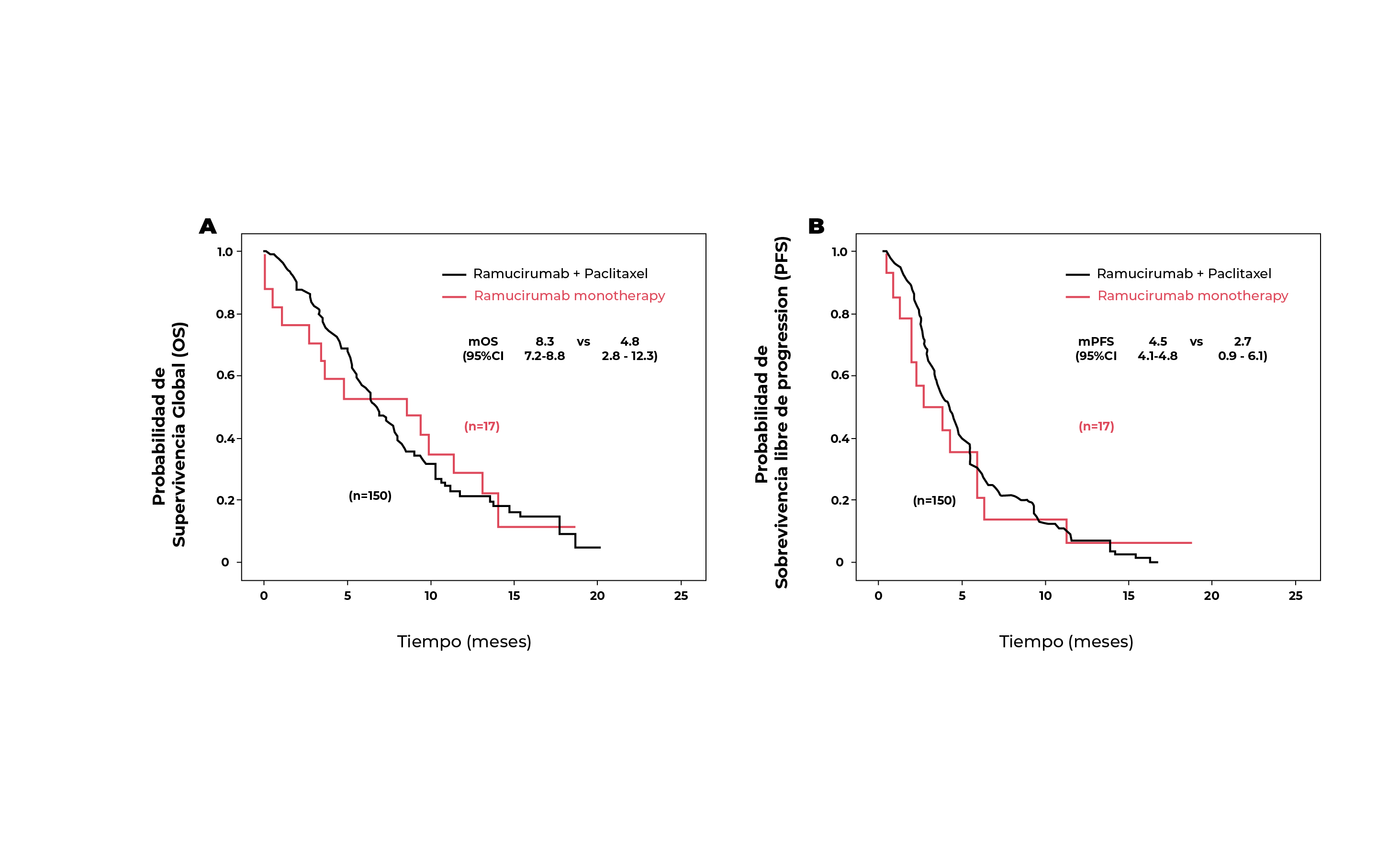
Estos datos de eficacia “en la vida real” sobre el tratamiento con ramucirumab están en línea con los ensayos aleatorios anteriores. Ramucirumab es bien tolerado en la práctica clínica diaria.2
Además, los resultados observados en los estudios REGARD y RAINBOW que muestran la eficacia de ramucirumab en todos los subgrupos de pacientes, con un buen perfil de seguridad, indican que ramucirumab solo o combinado con paclitaxel es una estrategia primaria en el panorama terapéutico del CG metastásico.2
Sin embargo, dado el resultado muy diferente entre el tratamiento combinado y la monoterapia, proponemos que los pacientes con un buen estado de desempeño (PS) sean candidatos para la terapia con ramucirumab y paclitaxel. Aunque este estudio presenta varias limitaciones, incluido su diseño retrospectivo y el análisis exploratorio de subgrupos, proporciona datos de resultados valiosos para pacientes tratados fuera de los ensayos clínicos, y los resultados obtenidos son consistentes con los estudios disponibles y brindan una confirmación adicional de que ramucirumab es efectivo y seguro. también en la práctica clínica de la vida real.2
Referencias:
- Wilke H, Muro K, Van Cutsem E, Oh SC, Bodoky G, Shimada Y, Hironaka S, Sugimoto N, Lipatov O, Kim TY, Cunningham D, Rougier P, Komatsu Y, Ajani J, Emig M, Carlesi R, Ferry D, Chandrawansa K, Schwartz JD, Ohtsu A; RAINBOW Study Group. Ramucirumab plus paclitaxel versus placebo plus paclitaxel in patients with previously treated advanced gastric or gastro-oesophageal junction adenocarcinoma (RAINBOW): a double-blind, randomised phase 3 trial. Lancet Oncol. 2014 Oct;15(11):1224-35. doi: 10.1016/S1470-2045(14)70420-6. Epub 2014 Sep 17. PMID: 25240821.
- Di Bartolomeo M, Niger M, Tirino G, Petrillo A, Berenato R, Laterza MM, Pietrantonio F, Morano F, Antista M, Lonardi S, Fornaro L, Tamberi S, Giommoni E, Zaniboni A, Rimassa L, Tomasello G, Sava T, Spada M, Latiano T, Bittoni A, Bertolini A, Proserpio I, Bencardino KB, Graziano F, Beretta G, Galdy S, Ventriglia J, Scagnoli S, Spallanzani A, Longarini R, De Vita F. Ramucirumab as Second-Line Therapy in Metastatic Gastric Cancer: Real-World Data from the RAMoss Study. Target Oncol. 2018 Apr;13(2):227-234. doi: 10.1007/s11523-018-0562-5. PMID: 29582224.



Lo sentimos, el formulario de comentarios está cerrado en este momento.